馬野弘之、佐佐木弘樹
硬質胃癌進展迅速,發現時往往為時已晚。因此,很難獲得用於研究的標本,並且治療方法的開發被推遲。此次,研究團隊首次利用患者腹水中所含的細胞對硬質胃癌進行了全面的基因組分析,並成功找到了治療標靶。我們訪問了進行這項研究的國家癌症中心研究所所長馬野博之和研究員佐佐木博樹。
--硬質胃癌是一種什麼樣的癌症?
馬諾先生: 硬性胃癌是一種難治性癌症,佔所有胃癌的5-10%。這是一種非常嚴重的癌症,往往會在黏膜下擴散,當確診時,它已經穿透胃壁並轉移到腹膜(腹膜播散),因此無法進行手術。
到目前為止,對於硬質胃癌的基因組分析或致癌機制的研究還沒有太大進展。在歐美,胃癌的發生率並不像日本那麼高。正因如此,硬質胃癌在以歐美為中心的癌症基因組計畫中並沒有受到太多關注,也沒有進行嚴格的分析。
使用從腹水中獲得的細胞
-- 這次,您在研究中使用了腹水中的癌細胞。
馬諾先生: 是的。腹膜是包圍體內胃和腸等內臟器官的膜。癌細胞轉移到腹膜,液體聚集在腹膜腔(腹膜包圍的空間)中。這稱為腹水。
在我們的研究中,我們能夠使用硬質胃癌患者的腹水。腹水含有侵入胃壁的癌細胞以及包括血球在內的各種其他細胞。我們對這些癌細胞進行了基因組分析。1。
-- 是什麼讓您決定使用腹水中的癌細胞?
馬諾先生: 佐佐木博士多年來一直從腹水中收集癌細胞。2017年,當我成為研究所所長時,我遇到了佐佐木博士,並得知他正在從腹水中收集癌細胞。我認為這是一個分析硬質胃癌的寶貴機會,所以我申請了聯合研究。
佐佐木先生: 我還記得當我解釋我的研究時,馬諾教授的眼睛閃閃發光(笑)。
——你從什麼時候開始收集它們的?
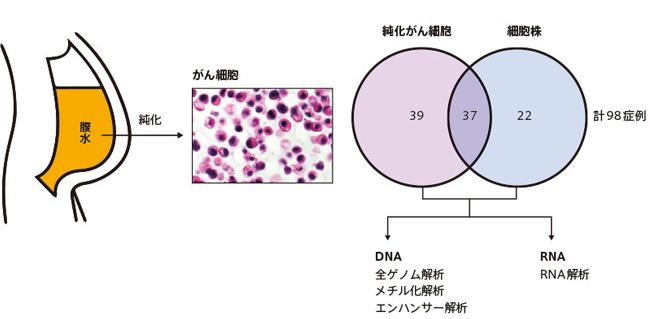
佐佐木先生: 時間已經是2010年左右了。我開始收集獨特的樣本,並將其用於研究。首先,在徵得每位患者同意的情況下,僅從腹水中去除癌細胞。這是純化的細胞。此外,我們也嘗試建立細胞系。將腹水中的全細胞沉澱在常規培養基中培養以建立細胞系。建立的細胞系(細胞系)很方便,因為它們可以無限地傳代培養。然而,建立細胞系的成功率約為30%,因此除了細胞系之外,我們還在本次分析中納入了冷凍保存的純化細胞。透過比較兩者的數據,您可以確認建立的細胞系的特徵反映了純化細胞系的特徵。
透過這種方式,我們能夠使用總共 98 名患者的癌細胞。
基因組分析帶來新發現
--您從基因組分析中學到了什麼?
馬諾先生: 我們使用下一代定序儀對 98 名患者的癌細胞的整個基因組進行了定序。然後,我們研究了所獲得的癌症基因組中包含哪種獲得性突變(體細胞突變)。
令人驚訝的是,硬質胃癌的基因組表現出高度的不穩定性。換句話說,這個基因組具有異常大量的高度擴增的基因。這是一個意外的發現。硬質胃癌屬於瀰漫性胃癌的一部分,而瀰漫性胃癌的特徵是基因組穩定性。
先前的癌症基因組計劃已針對手術標本進行分析,但由於硬質胃癌很少適合手術,我想標本無法獲得,並且往往被排除在範圍之外。我是。另外,在硬質胃癌的情況下,胃壁的纖維化進展,因此即使獲得樣本,預計樣本中癌細胞的比例也會較低。結果我們發現先前的癌症基因組計畫並不能準確掌握硬質胃癌的特徵。
--你有什麼樣的基因突變?
馬諾先生: 在受體酪胺酸激酶-RAS/MAPK路徑基因組中發現了許多特別高水平的基因擴增,該基因參與細胞增殖的調節。另外,我之前發現2還有一種導致肺癌的 EML4-ALK 基因融合。基因融合是兩個基因連結的突變。
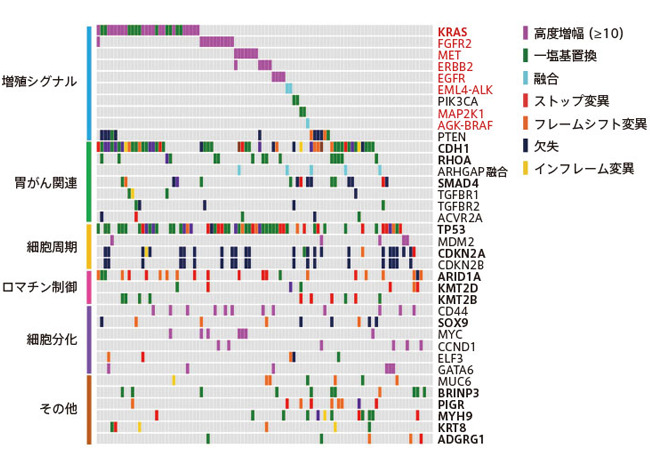
基因擴增、基因融合等突變數量較多,是基因組不穩定的一個特徵,也是易於轉移的硬質胃癌的一個可以理解的特徵。
同樣令人欣慰的是,針對此處發現的許多突變,已經存在其他癌症分子標靶藥物。分子標靶藥物針對突變分子,因此無論癌症類型如何,它們都有效。發現基因擴增和基因融合的基因佔所有硬胃癌病例的50%,其中一半病例已經有分子標靶藥物。
我們實際上使用幾種分子標靶藥物和個別小鼠進行了實驗,以確認藥物的有效性。我們要求佐佐木實驗室使用細胞和個體進行實驗。
-- 您也進行了轉錄組分析。
馬諾先生: 我們進行了多層轉錄組分析、增強子分析等,並闡明了以下內容。
首先,根據與上皮間質轉化(EMT)相關的基因的表達水平,硬質胃癌細胞可分為兩類。 EMT是指當癌症發生轉移時,它會失去其作為上皮細胞的原有特性(如細胞間黏附能力),並獲得間質細胞的特性(如侵襲性和迷走神經能力)。
在EMT基因高表現的組別中,發現了特徵性的超級增強子區域(控制基因表現的增強子集中的地方)。未來,對這種超級增強劑的研究可能有助於開發治療藥物和闡明致癌機制。
此外,我們發現轉錄因子如 TEAD 因 EMT 基因表現增加而被活化。 已知 TEAD 參與器官大小調節和致癌作用,我們證實 TEAD 抑制劑對這些胃癌有效。
擴大癌症基因組醫學的應用
——現有的一些分子標靶藥物和抑制劑是有效的,因此有望應用於癌症基因組醫學。
馬諾先生: 正如我之前提到的,我們的分析結果顯示,四分之一的硬質胃癌存在基因突變,而現有的分子標靶藥物對這些突變有效。我們希望在一年內進行臨床試驗,使這些現有藥物能夠用於治療硬胃癌。此外,由於尚未有 TEAD 抑制劑在臨床試驗中獲得批准,我們希望繼續進行研究和開發。
癌症基因組醫學於 2019 年在日本興起。這是一種使用稱為「基因組測試」的測試方法來找出患者的癌症基因組中存在哪些突變,然後為該人使用最合適的分子標靶藥物的醫療方法。由於可用的藥物還很少,我希望許多研究人員積極進行像這樣的分析,隨著結果的積累,可以治療的患者數量將會增加。
——這項研究的基因組資訊是公開的。我們希望研究也能從這個角度繼續發展。
佐佐木先生: 是的。這些資訊是公開的,任何人都可以透過諮詢資料註冊者(主要作者田中洋介,國家癌症中心研究所的研究科學家)來使用。我們相信這項研究作為研究資源非常有價值。這是因為細胞系、基因組資訊和臨床資訊是連在一起的。細胞係也可用於研究和開發,此類資源在藥物發現領域稱為生物資產。相信未來硬質胃癌的研究將會進一步發展。
-- 從腹水中收集癌細胞和細胞系的秘密是什麼?
佐佐木先生: 是興趣和熱情嗎?由於我長期在國家癌症中心工作,能夠穩定地進行採集癌細胞的基礎研究。到目前為止,在我的實驗室接受過培訓的許多年輕醫生現在都在全國的核心醫院工作。透過他們的轉介,獲得患者的腹水樣本並用於研究。
在收集癌細胞時,重要的是要考慮什麼對研究來說是重要的,而不是僅僅盲目地收集它們。難治性癌症的胰臟癌和日本快速增加的卵巢癌也容易引起腹水,所以我收集這些癌症的腹水並收集純化的癌細胞和癌細胞系,我們有庫存。這些基因組分析尚未完成。
——當您回顧這項研究時,您有什麼想法?
佐佐木先生: 我真的很幸運能夠與馬諾教授和他的同事們進行共同研究。甚至在此之前,我們就已經進行了部分基因組分析。然而,不可能進行像這樣的全面的多層組學分析,因此研究結果也很有限。
基因組分析工作可以外包,但是為了完成後續的數據分析,包括多次重新分析,直到得到足夠的結果,這種聯合研究是必要的,我認為這是不可能的。
馬諾先生: 僅使用外包的基因組數據來編譯此類研究肯定很困難。我們一開始也遇到了很多不順利的事情。當我嘗試各種事情時,這帶來了新的發現,進而帶來了更多的新發現。
檢驗抑制劑有效性的唯一方法是透過實驗一一測試,但我很高興最終我們能夠獲得與臨床實踐直接相關的結果。我長期從事癌症基礎研究,但我工作的核心始終是治癒患者的強烈慾望。所以我對這個結果非常滿意。
- 非常感謝。
訪談者是藤川涼子(科普作家)。
作者簡介

馬野弘之
美國國家癌症中心研究所細胞資訊學系主任
1984年畢業於東京大學醫學部。完成內科住院醫師訓練後,於1992年獲得醫學博士學位。他曾擔任自治醫科大學醫學院和東京大學醫學研究科教授,並於 2016 年就任現職。

佐佐木弘樹
美國國家癌症中心研究所基礎臨床開發研究核心中心(FIOC)藥物發現標靶與種子部研究員
1990年東京大學大學院農學研究科畢業(農業博士)。 1991年加入國立癌症中心研究所(當時)擔任研究員後,歷任部門經理和單位主任,2013年成為FIOC部門主任。 2020年退休並擔任現職。
參考書目
- Tanaka, Y. 等人,《自然癌症》2, 962–977 (2021)。
- 2 Soda, M. 等人,《自然》448, 561–566 (2007)。
* 本文轉載自《自然文摘》。
轉載自:自然文摘2022年第1期
“硬胃癌全基因組分析中的治療靶點“
自然文摘第 19 卷第 1 期 | doi: 10.1038 / ndigest.2022.220130
